Atombau + PSE Vorbereitung auf den MSA
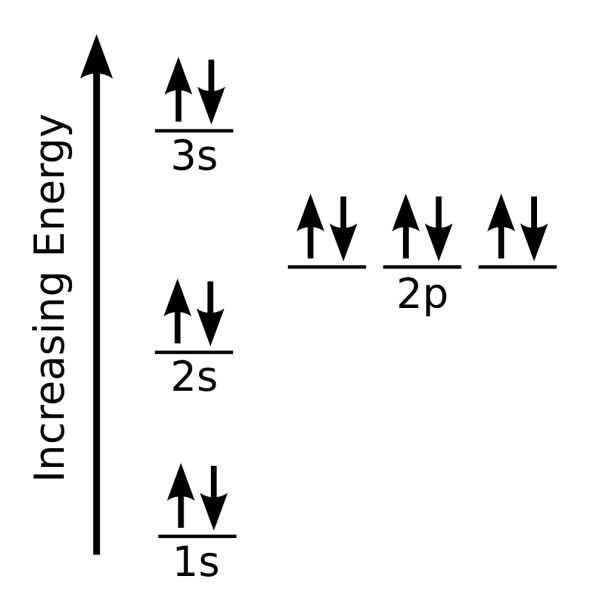
Die magnetische Quantenzahl m unterscheidet die Orbitale: m = 0 (ein s-Orbital) m = +1, 0, −1 (drei p-Orbitale) m = +2, +1, 0, −1, −2 (fünf d-Orbitale) m = +3, +2, +1, 0, −1, −2, −3 (sieben f-Orbitale) Die Spinquantenzahl s unterscheidet die beiden Elektronen in einem Orbital: s = +½, −½.
Magnesium Symbiosis Agriculture

Die Edelgaskonfiguration (seltener auch Edelgaszustand) bezeichnet eine Elektronenkonfiguration eines Atoms oder auch eines Ions, die der Elektronenkonfiguration des Edelgases der jeweiligen Periode entspricht. Mit Ausnahme der Elemente der ersten Periode ergibt sich so eine Konfiguration mit 8 Valenzelektronen .
File Electron Configuration Magnesium Svg Best Diagram Collection
Magnesium (Mg) hat zwei Elektronen. Dies ist aus seiner Elektronenkonfiguration ersichtlich. Die Valenzelektronen für Magnesium haben daher zwei. Die Wertigkeit ist ein numerisches Merkmal der Fähigkeit von Atomen eines bestimmten Elements, sich mit anderen Atomen zu verbinden. Die Wertigkeit von Wasserstoff ist konstant und gleich.
KernHülleModell
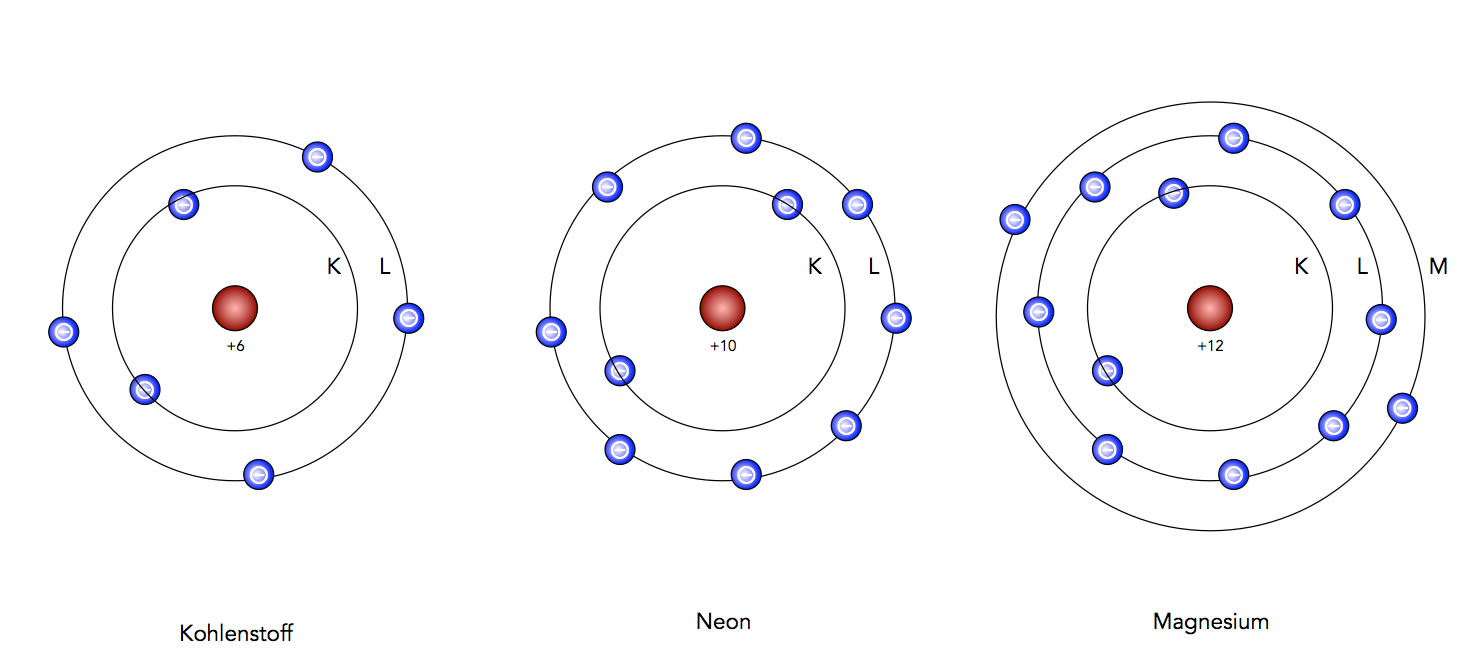
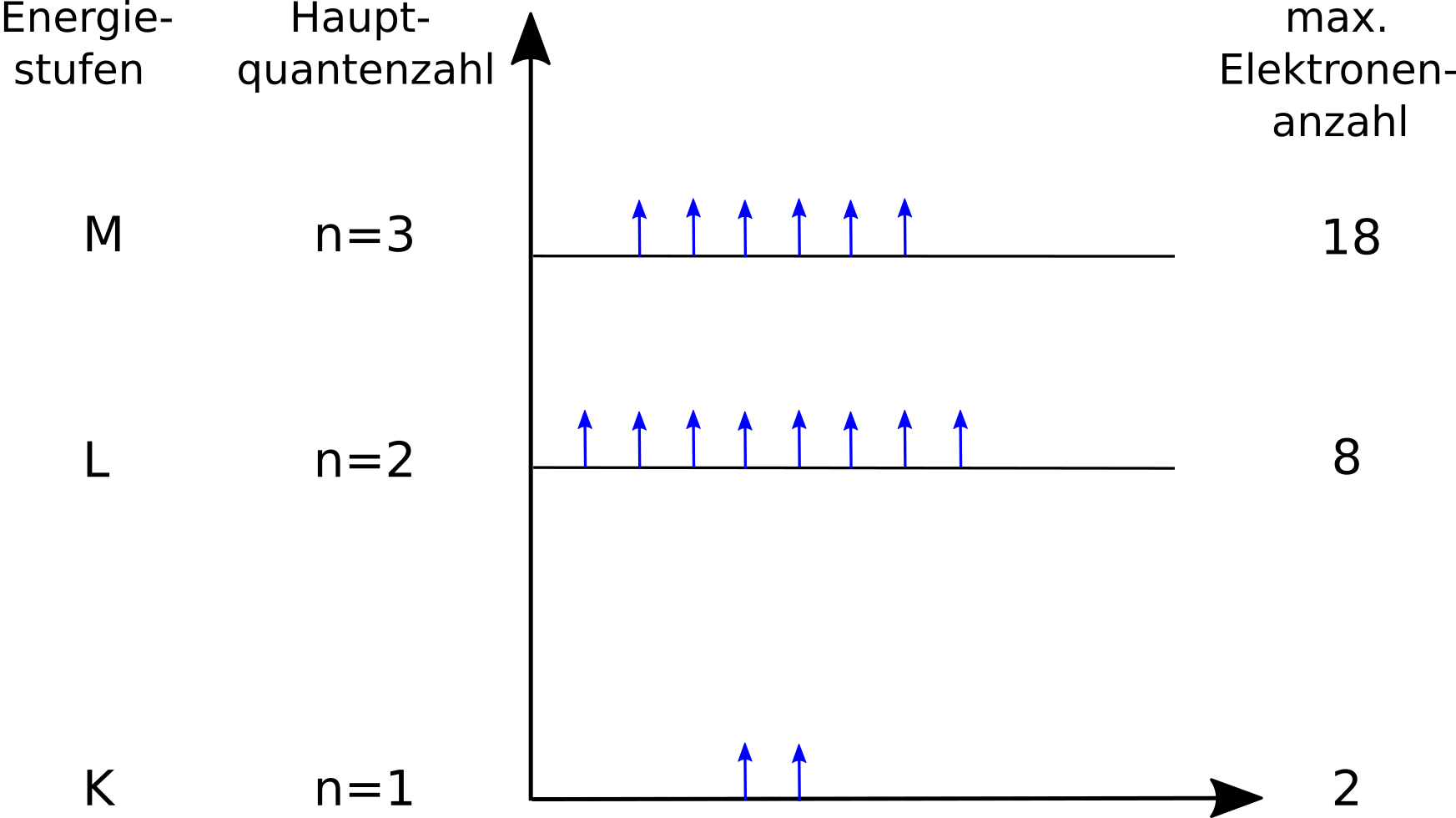
Atome mit bis zu 18 Elektronen. Bei allen Elementen mit 18 oder weniger Elektronen im Atom werden die Schalen einfach von innen nach außen mit Elektronen befüllt, jeweils so viele wie in der Schale hinein passen: Zwei Elektronen in die erste Schale, bis zu 8 in die zweite und 18 in die dritte Schale. Atome mit mehr als 18 Elektronen.
Model of magnesium atom stock vector. Illustration of mass 164475021
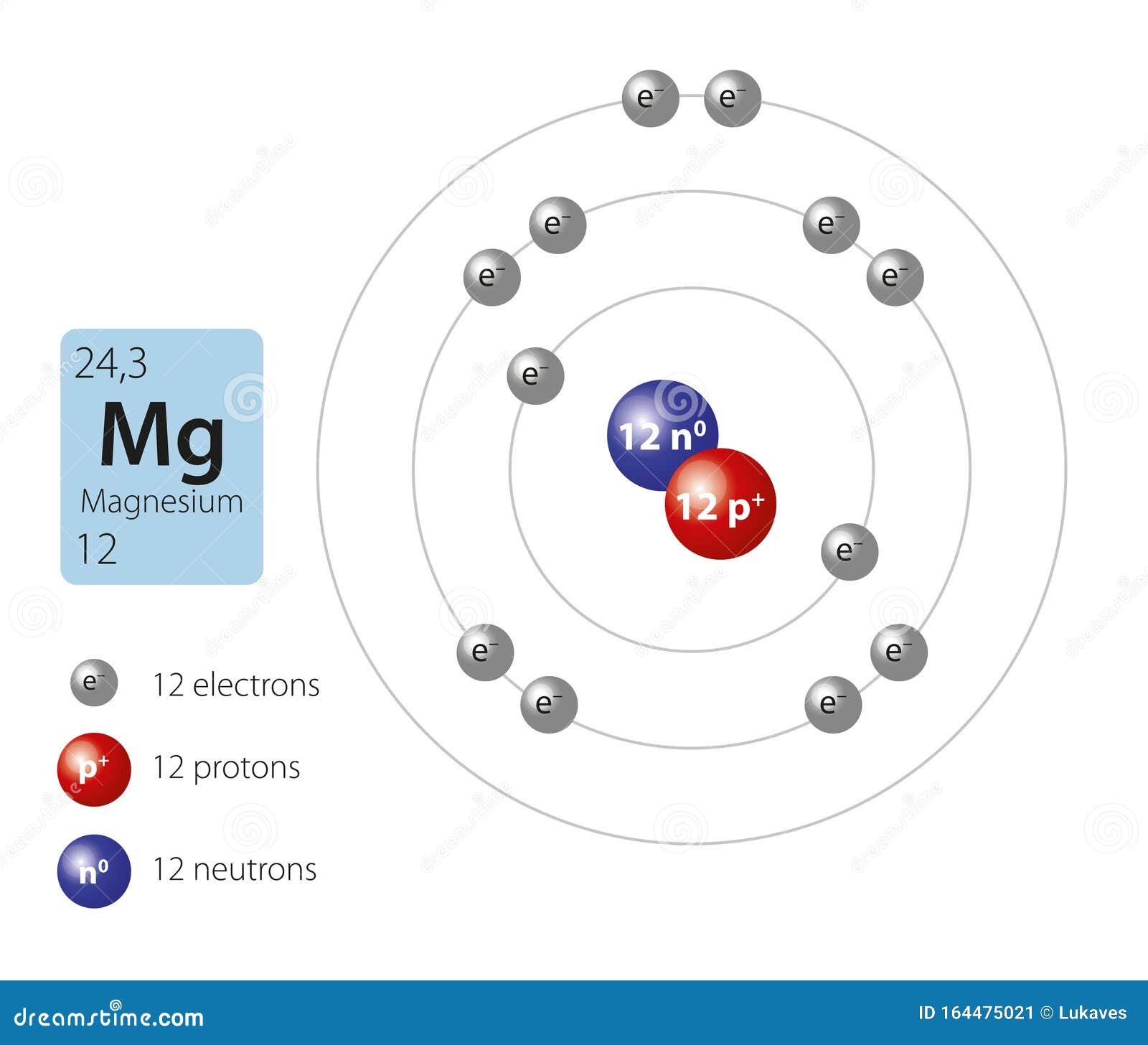
Damit du ein chemisches Element im Schalenmodell darstellen kannst, ist es wichtig zu wissen, wie viele Elektronen in eine Schale hineinpassen. Denn jede Schale kann nur eine bestimmte Anzahl von Elektronen aufnehmen. Denn die Schalen unterscheiden sich darin, wie viele Elektronen sich dort aufhalten können. Zusätzlich benennst du die Schalen.
Atombau + PSE Vorbereitung auf den MSA

Chemie und Physik des chemischen Elements Magnesium. Magnesium ist ein zu den Erdalkalimetallen zählendes chemisches Element der zweiten Gruppe des Periodensystems mit dem Elementsymbol Mg und der Ordnungszahl 12. In reinem Zustand ist das Metall ein glänzender, grauer Feststoff, der an der Luft durch Einwirkung des Sauerstoffs unter.
Magnesium XL Supersaturated formula
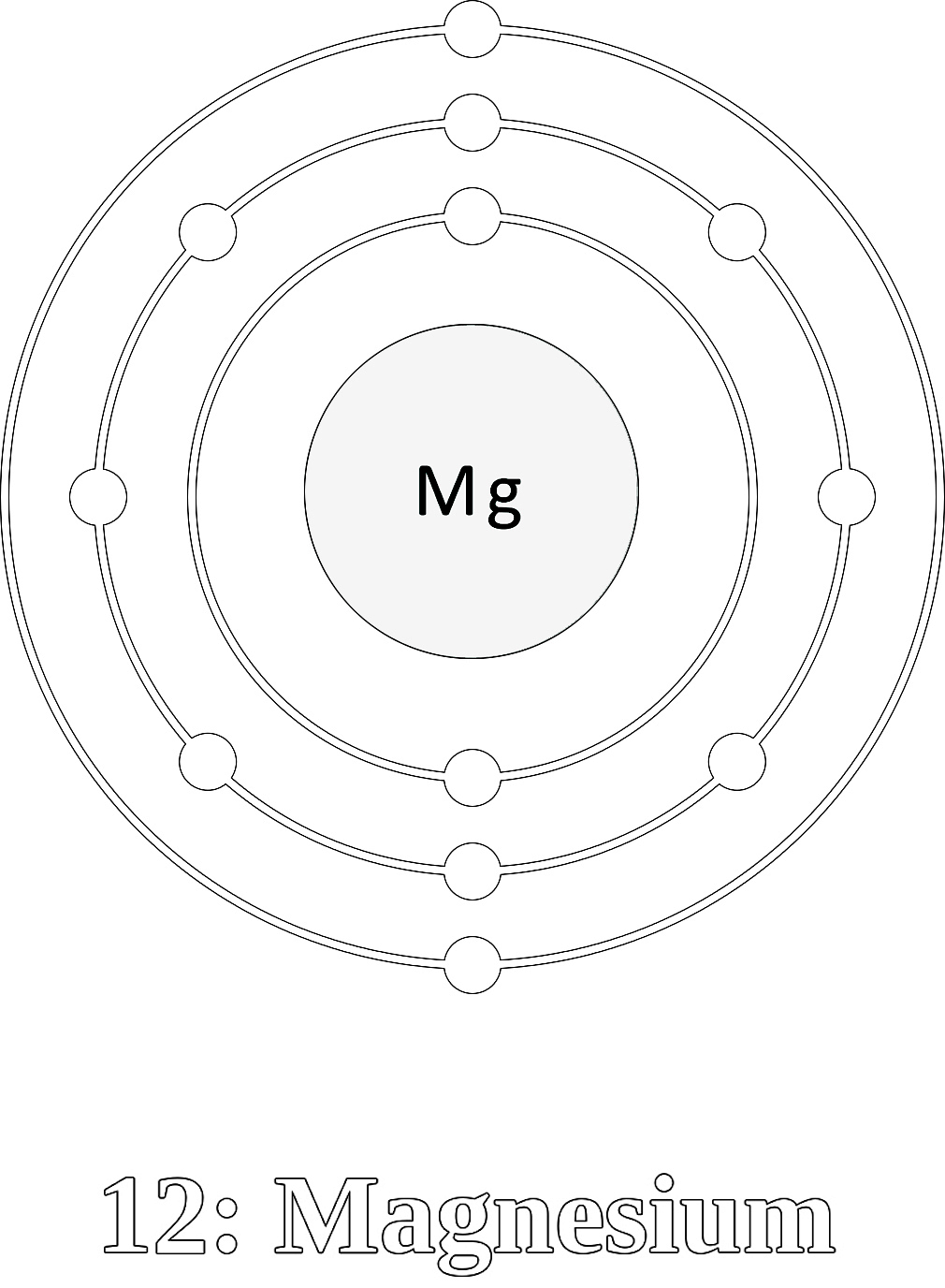
Ein Magnesium-Atom hat 12 Protonen im Kern und dementsprechend auch 12 Elektronen, verteilt auf die unterschiedlichen Schalen: Magnesium ist silbrig weiß und sehr leicht.
Atombau + PSE Vorbereitung auf den MSA
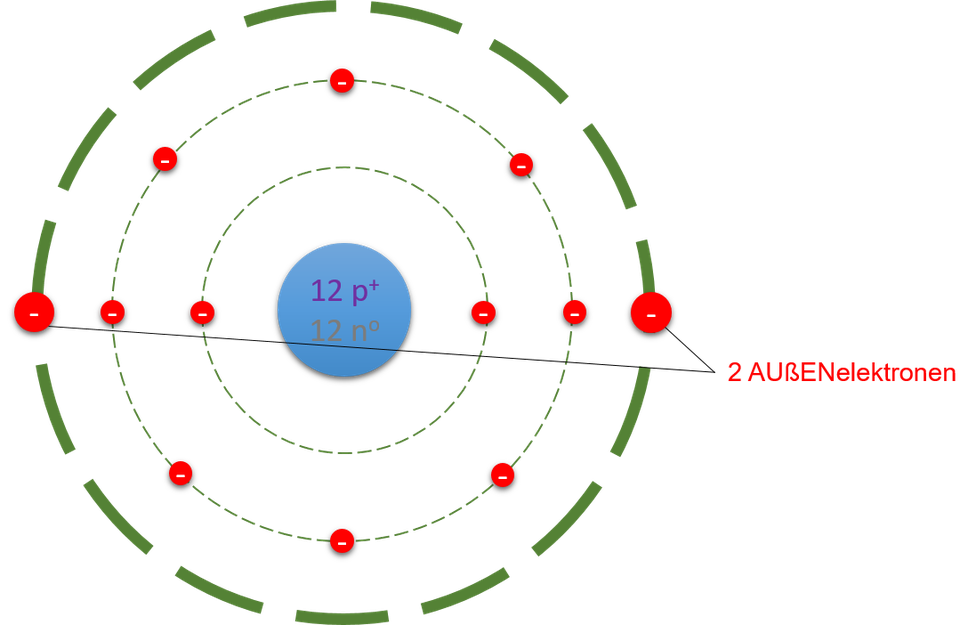
Das Magnesium-Atom gibt die beiden Außenelektronen ab und bildet. Für viele gilt daher Black als der eigentliche Entdecker des Magnesiums. 1808 gewann Humphry Davy durch Elektrolyse erstmals eine kleine Menge unreinen Magnesiums. 1829 wurde von dem französischen Chemiker Antoine Bussy (1794-1882) das Metall in reiner Form erhalten. Sir Humphry Davy (1778-1829) Quelle: Epsom and Ewell.
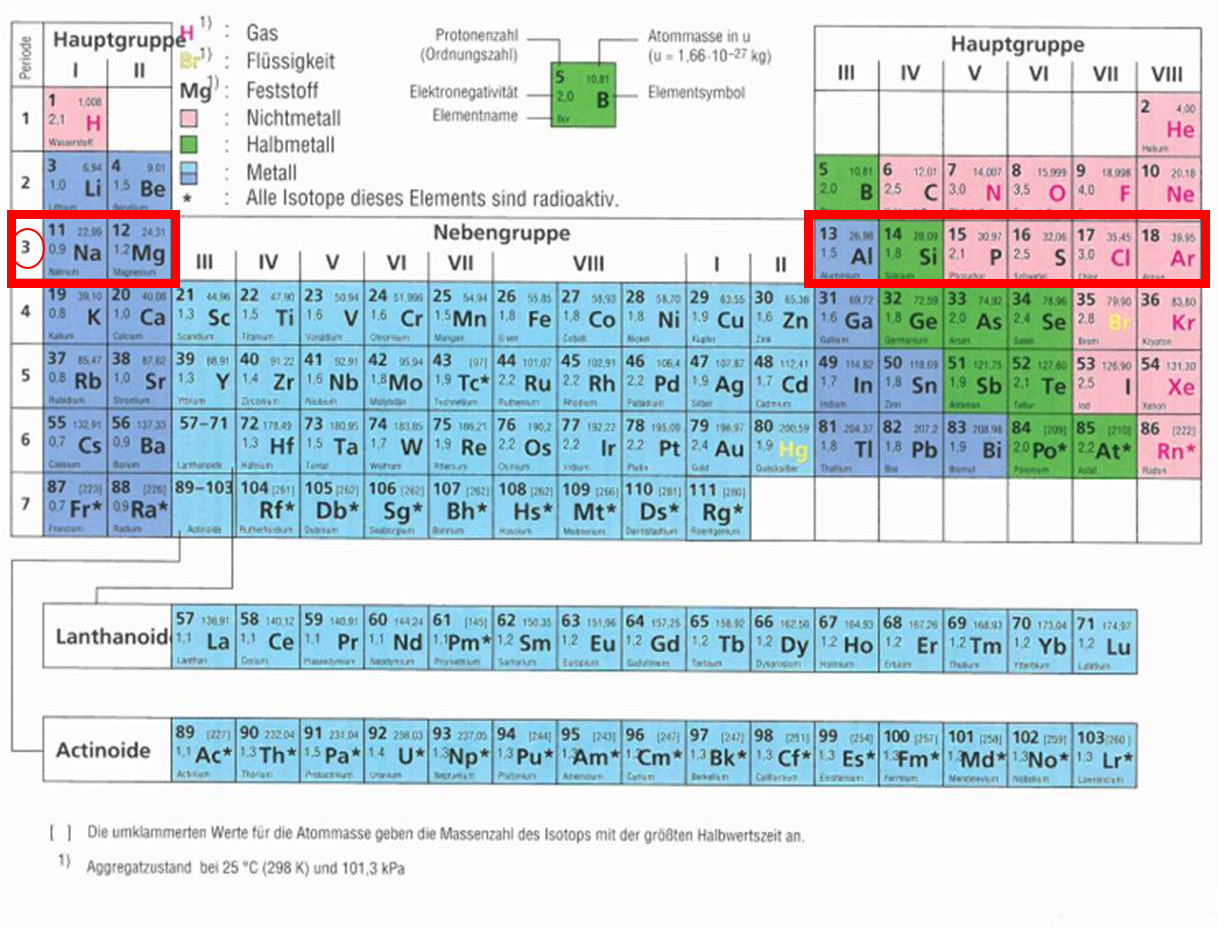
Das Periodensystem der Elemente lernen mit Serlo!
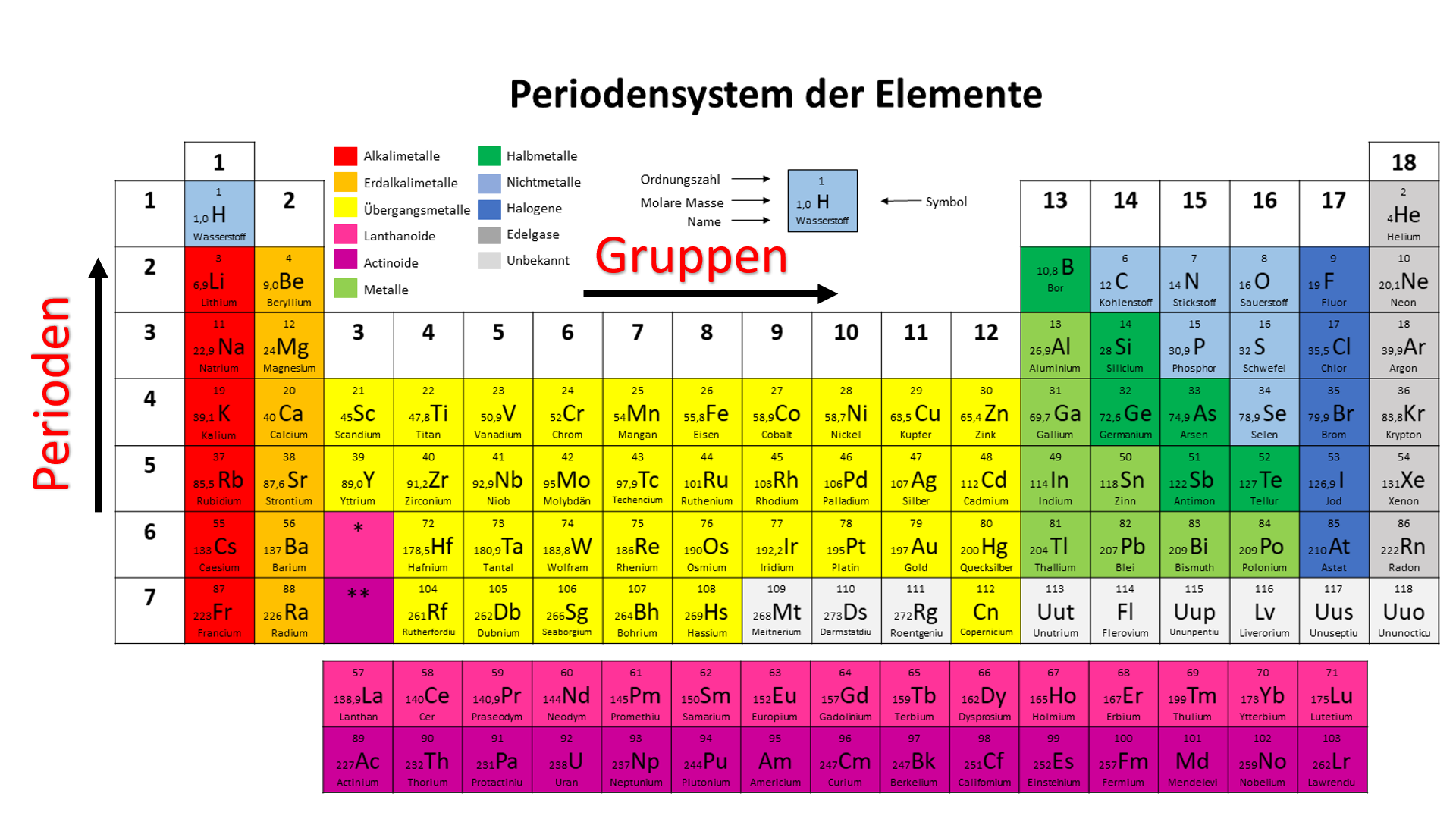
Magnesium ist ein chemisches Element mit dem Elementsymbol Mg (Alchemie: ⚩) und der Ordnungszahl 12. Im Periodensystem der Elemente steht es in der zweiten Hauptgruppe bzw. der 2. IUPAC-Gruppe und gehört damit zu den Erdalkalimetallen. Magnesium ist eines der zehn häufigsten Elemente der Erdkruste.Es kommt in zahlreichen Mineralen, im Meerwasser, sowie im Blattgrün der Pflanzen vor.
Magnesium, atomic structure Stock Image C018/3693 Science Photo Library Electron

Es hat zwei Außenelektronen (Valenzelektronen), wodurch die Chemie des Magnesiums bestimmt wird. Als achthäufigstes Element ist es zu etwa 1,94 % am Aufbau der Erdkruste beteiligt. Geschichte. Die Herkunft der Elementbezeichnung wird in der Literatur unterschiedlich dargestellt: von altgriech. μαγνησιη λιθός in der Bedeutung „Magnetstein",
Freies Lehrbuch Chemie" 06 Atombau Das KernHuelle Modell und das Periodensystem
Heutzutage wird Magnesium hauptsächlich aus magnesiumhaltigen Mineralien gewonnen, wie zum Beispiel Magnesit, Dolomit oder Olivin. Die größten Förderer von Magnesium sind China, Russland, Israel und Brasilien. Magnesium verfügt über eine Atommasse von 24,305 u und einem Atomradius von 150 pm, wobei der kovalente Radius 141 pm beträgt.
Magnesium Facts

1.31. Atomradius / pm: 159.9. Relative atommasse: [24.304, 24.307] 1808 Sir Humphry Davy (GB) Der Name Magnesium leitet sich von Magnesia (Griechenland), einem Gebiet im östlichen Griechenland ab. Magnesium ist ein glänzt silberweiß Leichtmetall, überzieht sich an der Luft mit einer dünnen Oxidhaut (Passivierung) und verbrennt mit.
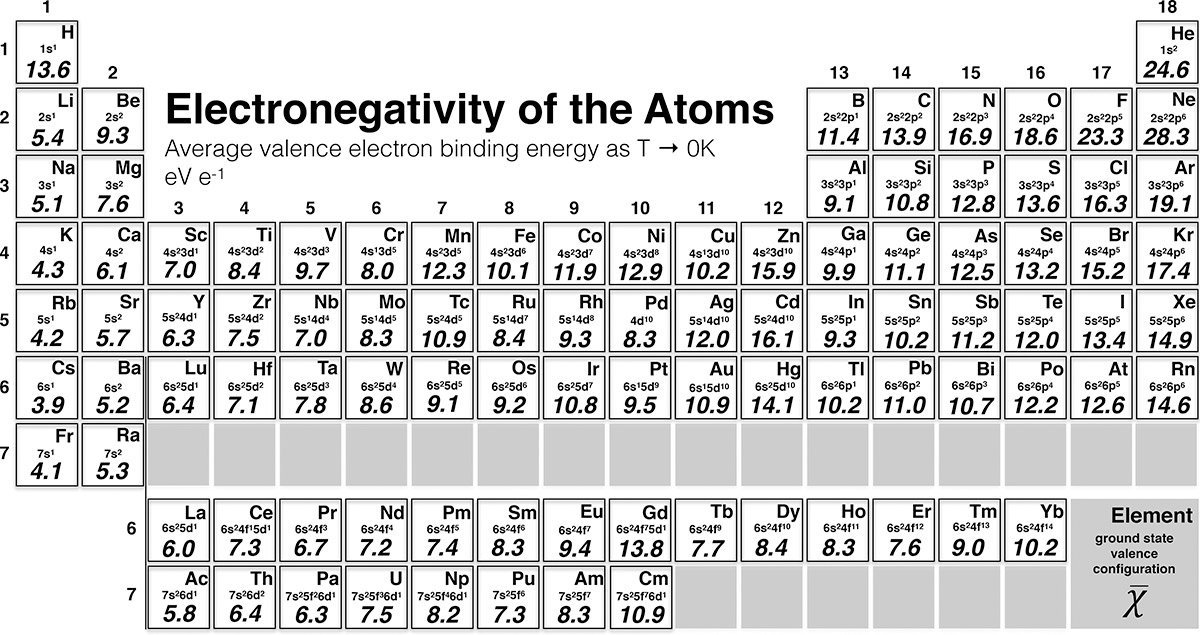
Neue Definition der Elektronegativität Forscher entwickeln neue Skala der Elektronenanziehung
Reines Magnesium ist weich, hat nur eine geringe Festigkeit und ist zudem sehr korrisionsanfällig. Das Metall überzieht sich an Luft mit einer grauen Oxidschicht, die es allerdings vor weiteren Reaktionen schützt. Magnesium ist brennbar. Bei der Verbrennung wird sehr viel Energie in Form von Wärme, aber auch als Lichtenergie abgegeben.
magnesium electron configuration Newton Desk
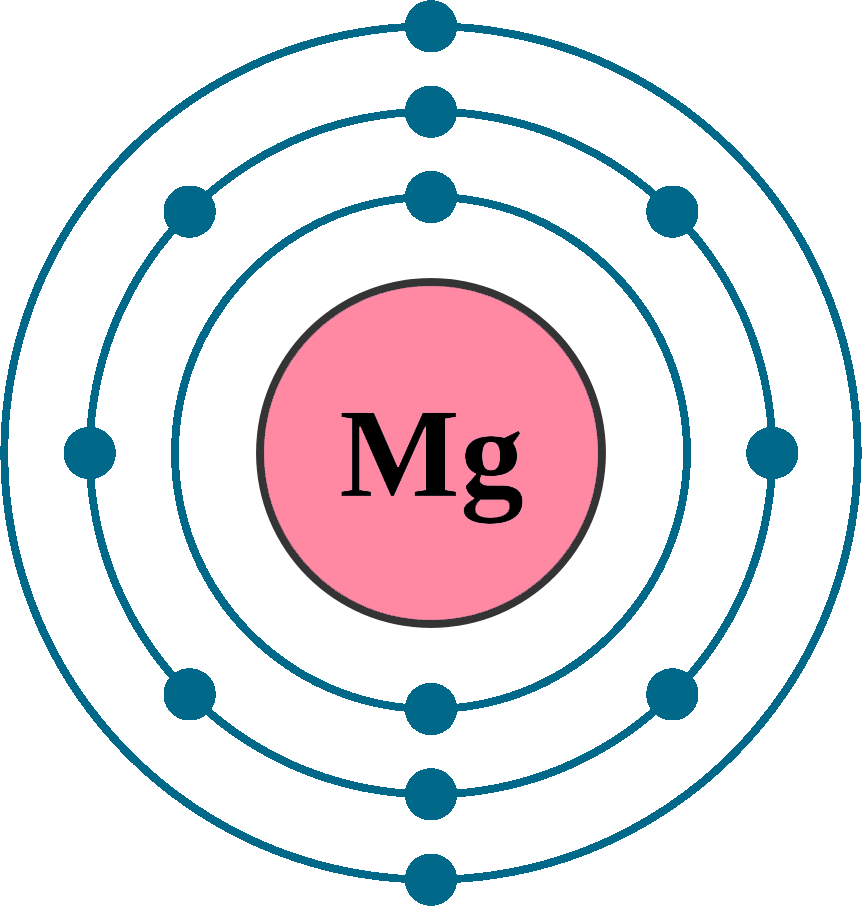
Magnesium, Mg, Element der Hauptgruppe II des Periodensystems, den Erdalkalimetallen. Magnesium besitzt die Elektronenkonfiguration [Ne]3s 2 und kommt in 12 Isotopen vor. Technische Verwendung findet Magnesium hauptsächlich als Bestandteil von leichten Legierungen (Flugzeug- und Automobilbau).
FileElectron shell 012 Magnesium.svg

Von zehn Magnesium-Atomen sind durchschnittlich acht 24 Mg, eines 25 Mg und eines 26 Mg. Magnesium wird im Universum durch das Kohlenstoffbrennen als Hauptprodukt gebildet. Dabei fusionieren zwei Kohlenstoff-12-Kerne zu einem Magnesium-24-Kern. Der Großteil der beiden schweren Magnesium-Isotope wird durch p-Prozesse sukzessive aus Mg-24.
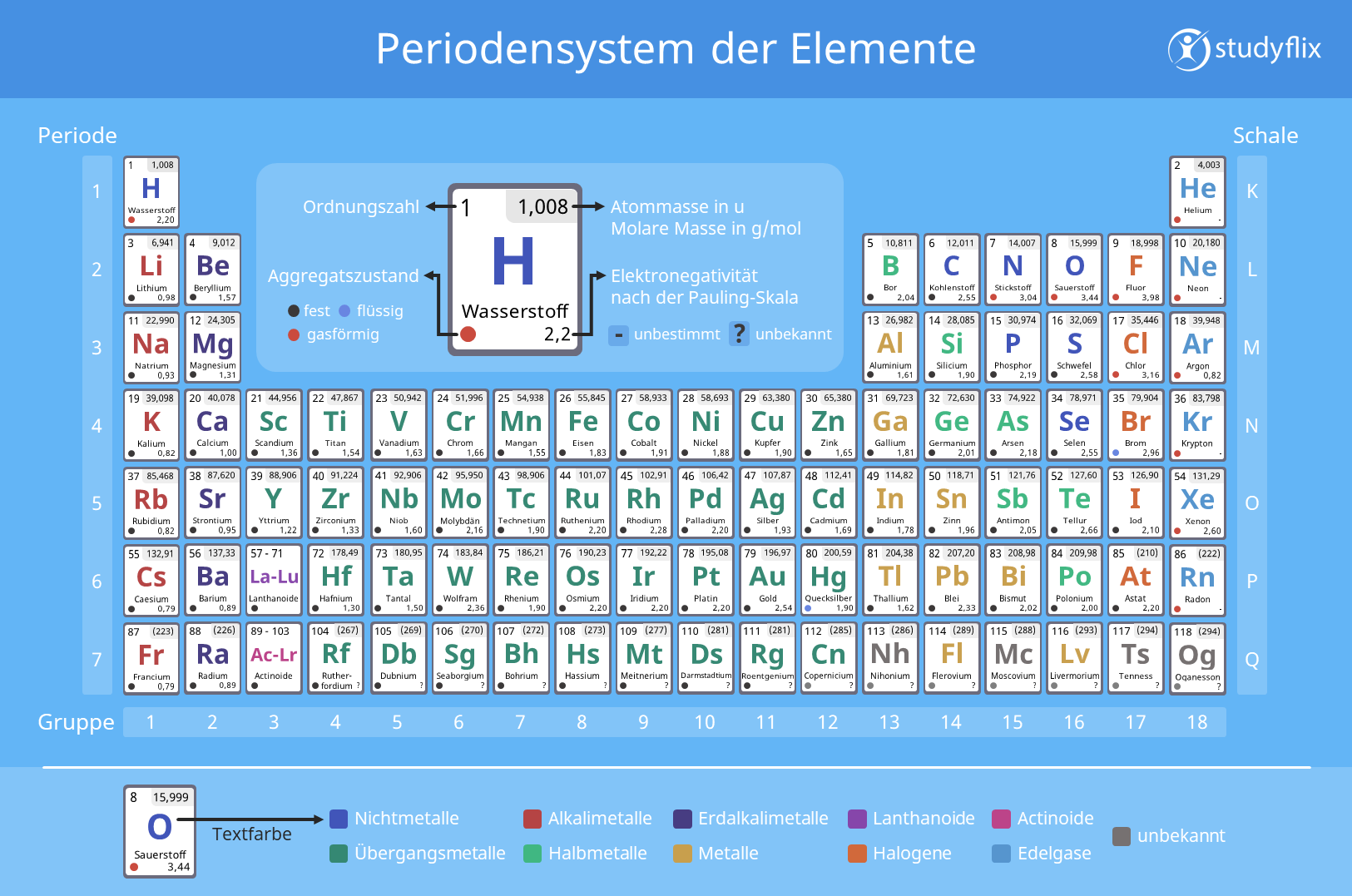
Periodensystem • Übersicht, chemische Elemente · [mit Video]
Liste, Daten und Eigenschaften aller bekannten natürlichen und künstlichen Isotope des Magnesiums sowie radioaktive Zerfallsprodukte bzw. Zwischenprodukte. Von den 22 bekannten Isotopen des Magnesiums treten 3 als stabile Kerne in der Natur auf: 24 Magnesium, 25 Magnesium und 26 Magnesium. Alle anderen Magnesiumisotope sind instabile.